A Ansiedade pode estar Naturalmente Enraizada no Cérebro Durante a Gravidez

Créditos da imagem: Pixabay
Um novo estudo descobriu que o estresse vivenciado durante a gravidez pode reprogramar o cérebro do bebê, aumentando o risco de ansiedade. Condições negativas antes do nascimento alteram o desenvolvimento dos neurônios no hipocampo, tornando a criança mais sensível a ameaças mais tarde na vida.
De acordo com a Organização Mundial da Saúde (OMS), os transtornos de ansiedade são a condição de saúde mental mais prevalente em todo o mundo. Embora reagir ao perigo seja um mecanismo natural de sobrevivência, reagir exageradamente a ameaças percebidas é prejudicial. Isso levanta a questão: essas reações intensificadas são inerentes ao nascimento ou adquiridas pela experiência?
O Estresse Pré-Natal pode Reprogramar o Cérebro, Aumentando o Risco de Ansiedade mais Tarde na Vida
Pesquisadores da Weill Cornell Medicine (WCM) lançaram um novo estudo para examinar se a exposição a condições adversas durante o desenvolvimento — como inflamação e infecção — leva à ansiedade mais tarde na vida.
“Nossas descobertas mostram que a adversidade pré-natal causa alterações duradouras nos neurônios do giro dentado ventral (vDG), conectando o ambiente gestacional a comportamentos semelhantes à ansiedade”, disse o Professor Miklos Toth, MD, PhD, coautor correspondente e Professor de Farmacologia. “Esse processo pode ajudar a explicar por que alguns indivíduos com ansiedade inata apresentam sensibilidade e evitação contínuas ao estresse.”
O giro dentado ventral (vDG), uma parte do hipocampo, regula ativamente o processamento emocional e as respostas ao estresse, associando-o intimamente à ansiedade. Para estudar isso, os pesquisadores utilizaram um modelo murino para replicar um ambiente pré-natal adverso, especificamente a ativação imunológica materna, que simula infecção ou inflamação durante a gravidez, e observaram seu impacto nas células vDG.
O Estresse Pré-natal pode Reconectar o Cérebro, Aumentando o Risco de Ansiedade mais Tarde na Vida
Eles utilizaram uma série de técnicas — realizando testes comportamentais, registrando a ativação e a comunicação neuronal por meio de eletrofisiologia, analisando a metilação do DNA para rastrear alterações na regulação gênica, sequenciando RNA para identificar genes ativados ou suprimidos em neurônios específicos e aplicando fotometria de fibras para monitorar a atividade neural em tempo real em situações seguras e ameaçadoras.
Filhos de camundongos expostos a condições estressantes ou adversas durante a gestação apresentaram aumento de comportamentos semelhantes à ansiedade. Nesses camundongos, os pesquisadores descobriram que as células granulares dentadas ventrais (vDGCs) apresentaram inibição reduzida, resultando em maior excitabilidade. O ambiente pré-natal estressante alterou a expressão gênica nos neurônios dos filhotes, modificando marcadores químicos em seu DNA (metilação do DNA). Essas mudanças impactaram principalmente os genes envolvidos na conectividade e comunicação neuronal.
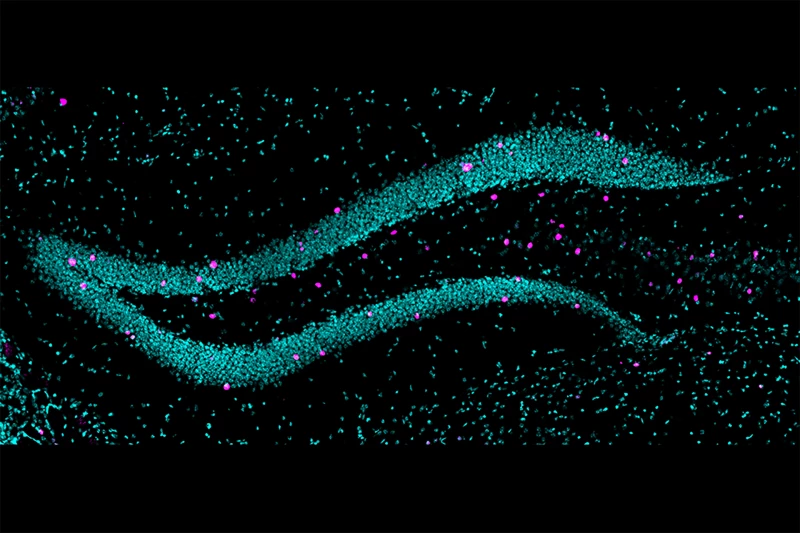
Faixas densas de neurônios (coloridos em azul-petróleo) nas duas lâminas do vDG. As células coradas em rosa foram hiperativadas quando o camundongo entrou em um ambiente ameaçador, indicando comportamento de evitação e ansiedade elevada. Weill Cornell Medicine/Nicole Politowska
Alterações Cerebrais Aumentam a Percepção de Ameaça em Camundongos Expostos ao Estresse
Quando os camundongos foram colocados em situações estressantes ou indutoras de ansiedade, as células cerebrais com essas alterações tornaram-se as mais ativas. Nessas células, muitos genes relacionados às conexões neurais funcionavam de forma diferente do normal. Observações em tempo real das células granulares dentadas ventrais (vDGCs) revelaram que camundongos expostos à adversidade apresentaram atividade aumentada durante a transição de ambientes seguros para ambientes ameaçadores, indicando uma maior percepção de ameaça.
“De modo geral, essas modificações epigenéticas fazem com que neurônios específicos nas vDGs reajam de forma diferente na idade adulta ao se depararem com ambientes inseguros”, explicou Kristen Pleil, PhD, Professora Associada de Farmacologia na WCM e coautora correspondente do estudo. “Esses neurônios tornam-se hiperativos, levando os camundongos a interpretar o ambiente ao seu redor como mais perigoso do que realmente é.”
Limitações do Estudo Reconhecem a Necessidade de Pesquisa, mas Reforçam a Ligação entre Estresse e Ansiedade Pré-Natal
O estudo apresenta algumas limitações. Como os pesquisadores realizaram o estudo em camundongos, os resultados podem não se aplicar diretamente aos humanos. Os efeitos variaram entre os neurônios, com apenas cerca de 10% a 30% das células apresentando alterações significativas na metilação. Além disso, o estudo não estabeleceu definitivamente quais alterações na metilação levaram a alterações transcriptômicas específicas, uma questão que requer investigação mais aprofundada. A pesquisa se concentrou no giro dentado ventral (vDG), embora outras partes do hipocampo também possam desempenhar um papel.
Apesar dessas limitações, o estudo corrobora a noção de que a inflamação materna ou o estresse durante a gravidez podem aumentar o risco de transtornos de ansiedade nos filhos mais tarde na vida. Os pesquisadores sugerem que seu trabalho oferece uma das conexões mecanísticas mais claras até o momento entre o ambiente pré-natal, modificações epigenéticas e condições psiquiátricas.
“O giro dentado ventral (vDG) de um camundongo contém quase 400.000 células, mas apenas alguns milhares são afetados durante a gravidez”, explicou Toth. “Nosso próximo objetivo é descobrir por que essas células específicas passam por programação epigenética.”
Leia o Artigo Original New Atlas










