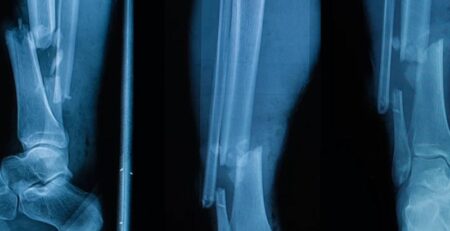
O Ciclotron Resgata a Tabela Periódica Quando a Física Fica Caótica

Créditos da imagem: O grupo dos actinídeos da tabela periódica Laboratório de Berkeley
Pesquisadores do Laboratório Nacional Lawrence Berkeley, do Departamento de Energia, contam com o Ciclotron de 88 Polegadas para estabilizar a tabela periódica, átomo por átomo, onde as coisas se tornam imprevisíveis na extremidade dos elementos pesados.
O Legado da Tabela Periódica na Sala de Aula
Para muitas pessoas, a tabela periódica traz lembranças de aulas de ciências monótonas, com seu pôster gigante servindo como distração das aulas e uma alternativa para cochilar. Mas, além de seu papel como decoração de parede, esta tabela com arranjos peculiares representa um dos avanços mais profundos da história científica.
Introduzida pela primeira vez em 1869 pelo químico russo Dmitri Mendeleev, e posteriormente refinada, a tabela organizou com sucesso os elementos de acordo com o peso atômico e as propriedades. Sua verdadeira genialidade, no entanto, residia em seu poder preditivo — permitindo aos cientistas prever as propriedades de elementos que ainda não haviam sido descobertos.

O espectrômetro de massa FIONA do Berkeley Lab
Essa previsão deu aos químicos uma grande vantagem. Por exemplo, astrobiólogos especularam que a vida alienígena poderia usar silício em vez de carbono ou respirar cloro em vez de oxigênio, tudo graças aos padrões revelados pela tabela.
Quando Elementos Pesados Quebram as Regras
Ainda assim, o sistema começa a falhar com elementos muito pesados — particularmente aqueles além do número atômico 99. Nessa escala, os elétrons orbitam o núcleo a velocidades próximas à da luz, desencadeando efeitos relativísticos descritos por Einstein. O aumento de sua massa puxa suas órbitas para dentro, reorganizando outros elétrons e distorcendo o comportamento químico esperado dos elementos.
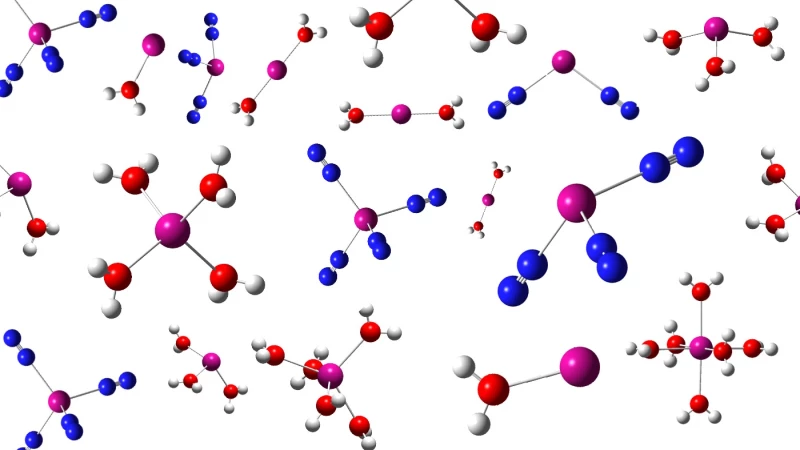
Moléculas de nobélio formadas com nitrogênio e água Laboratório de Berkeley
Em suma, quando os elementos se tornam extremamente pesados, sua química se torna menos previsível, deixando os cientistas dependentes de experimentos diretos em vez de suposições teóricas. Mas há um desafio: esses elementos transurânicos não ocorrem naturalmente, decaem quase instantaneamente e são intensamente radioativos. Por exemplo, o Nobélio (elemento 102) sobrevive no máximo 58 minutos antes de desaparecer. Isso significa que os experimentos devem ser realizados em meros milissegundos.
Para resolver isso, os cientistas do Laboratório Berkeley reviveram um cíclotron construído em 1958. Emparelhado com um espectrômetro de massa conhecido como FIONA, o sistema bombardeia alvos de túlio e chumbo com isótopos de cálcio para gerar átomos como nobélio e actínio (elemento 89).
Moléculas Nascidas em Velocidades Supersônicas
Inesperadamente, esses átomos fugazes formaram moléculas com traços de água e nitrogênio ao saírem do cíclotron em velocidades supersônicas. A FIONA então os analisou, átomo por átomo, medindo as massas moleculares em tempo real.
A escala é impressionante: após 10 dias, os pesquisadores haviam criado apenas cerca de 2.000 moléculas — um forte contraste com uma única gota d’água, que contém 10²¹ moléculas.
Isso abre as portas para a próxima geração da química átomo por átomo com elementos superpesados”, explicou Jennifer Pore, cientista do Laboratório Berkeley. “Isso pode remodelar completamente a forma como estudamos esses elementos exóticos — e até mesmo desafiar sua posição atual na tabela periódica.
Leia o Artigo Original New Atlas
Leia mais Treinamento de Drones para Navegar em Dutos de ar Como John McClane